Предложен новый механизм образования частиц наноалмаза при детонационном синтезе по следующей схеме: распад молекул тринитротолуола на основные радикалы – радикалоподобный димер С2 и СН3, молекул гексогена – на С2, молекул бензотрифуроксана – на С2; образование циклогексана из С2 или сразу молекул адамантана в радикальной форме; взаимодействие алмазоподобного ядра (радикала адамантана) с димером С2 и с метильным и другими моноуглеродными радикалами; рост частиц детонационного наноалмаза аналогично CVD — процессу. Показано, что зарождение радикалоподобных молекул адамантана происходит в диапазоне от середины зоны химпика до плоскости Чепмена — Жуге, одновременно растут алмазные частицы, их рост завершается в начальной стадии изоэнтропиного (телоровского) расширения газообразных продуктов детонации, захватывающих твердые частицы углерода.
Теория процесса, приводящего к образованию частиц детонационного наноалмаза (ДНА), все еще носит дискуссионный характер, и, по мнению авторов, отсутствует адекватная физико-химическая модель детонационного синтеза. Анализ наших данных и данных других авторов по результатам подрыва сплава тротила с гексогеном (~ 50/50) и безводородного бензотрифуроксана, тем не менее, позволяет постепенно подходить к пониманию механизма образования ДНА.
Детонационная волна представляет собой единый комплекс ударной волны, во фронте которой начинается разложение взрывчатого вещества (ВВ), зоны химической реакции (ЗХР), которая следует за ударной волной и заканчивается в плоскости Чепмена — Жуге, и, наконец, тейлоровской волны разгрузки (изоэнтропы). Причем энерговыделение продолжается и за плоскостью Чепмена — Жуге. Максимальные давление и температура достигаются внутри ЗХР.
ДНА образуются из химически связанного углерода, входящего в состав используемых ВВ.
Еще в [1] был обнаружен излом на кривой зависимости скорости детонации D от начальной плотности ρ0 тринитротолуола (ТНТ), который впоследствии был объяснен [2, 3] началом образования алмаза из “лишнего” углерода продуктов детонации (ПД) ТНТ в ЗХР (рис. 1). В [3] были зарегистрированы вторые изломы D(ρ0)-зависимости при подрыве сплавов ТНТ с гексогеном – ТГ 75/25 и ТГ 50/50, которые объясняли завершением образования алмаза. В районе изломов D(ρ0)-зависимостей ТНТ и ТГ 75/25 было зарегистрировано значительное возрастание электрического сопротивления ПД (RПД), связанное с образованием непроводящего алмаза вместо проводящих углеродсодержащих продуктов детонации [4, 5].
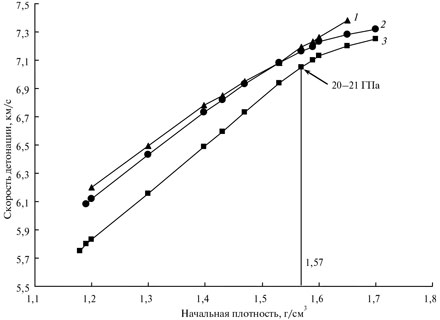
Рис. 1. Зависимости скорости детонации D от начальной плотности ρ0: 1 – ТГ 50/50; 2 – тетрил; 3 – пикриновая кислота.
С помощью электромагнитного метода измерения массовой скорости было определено давление в плоскости Чепмена — Жуге при плотности, соответствующей первому излому зависимости D(ρ0) тетрила. Оно составило ~ 20 – 21 ГПа [6]. Первый излом при использовании тетрила появляется при плотности заряда 1,57 г/см3.
Все большее отклонение зависимости D(ρ0) от первоначального хода обусловлено увеличением доли алмаза в углеродной фракции ПД. На достижение полноты превращения неокисленного углерода в алмазную фазу на зависимости D(ρ0) должен указать второй излом (в сторону бóльших D). Однако необходимого для этого давления нельзя создать даже при максимально возможной плотности ТНТ. Поэтому к ТНТ и добавляют более мощный гексоген [7].
Зависимость электросопротивления RПД ПД от ρ0 ВВ при значениях ρ0, отвечающих первым изломам D(ρ0)-зависимостей, должна проходить и проходит через минимум (рис. 2).
Анализ зависимости RПД от времени процесса показывает, что начавшееся в ЗХР образование алмаза продолжается и за ее пределами. Таким образом, можно считать доказанным, что процесс образования наноалмаза протекает в ЗХР и завершается в начале тейлоровского расширения ПД, т. е. в процессе разлета ПД кристаллиты ДНА сначала продолжают расти и только после резкого падения давления и температуры, снижения концентрации активных углеродных радикалов их рост прекращается. В целом определены параметры начала и завершения процессов образования ДНА. И если место образования ДНА достаточно определено, то из чего и как образуется кристаллит ДНА и почему прекращает свой рост – не ясно.
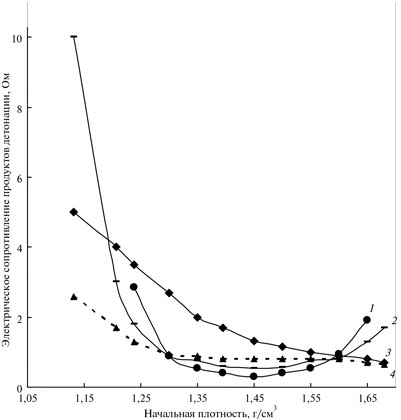
Рис. 2. Зависимости электрического сопротивления продуктов детонации от их начальной плотности: 1 – пикриновая кислота; 2 – тетрил; 3 – гексоген; 4 – ТГ 50/50.
Распад молекул ВВ обеспечивает довольно высокую концентрацию “свободного” углерода в ограниченной временем и объемом ЗХР – зоне химического пика (химпика), причем состав реакционной смеси непрерывно меняется. Плотность этой среды (“плазмы”) ~ 2,3 г/см3, она характеризуется высокой плотностью ионов, свободных электронов, простейших радикалов. При детонации углеродсодержащих ВВ в ЗХР образующаяся “плазма” попадает в область стабильности алмазной фазы, когда термодинамически выгодна химическая реакция перехода углеродсодержащих фрагментов исходных молекул ВВ в праструктуру алмаза, но невозможен развал образовавшихся зародышей.
Удобное для многих авторов [8–12] представление о том, что в детонационной волне (на самом деле, в зоне химпика) происходит полное разрушение молекул ВВ на атомы, не реально. Дело в том, что для разрыва только связей С–С, С–Н и С–N в ТНТ требуется ~ 23900 кДж/кг, а теплота взрывчатого разложения составляет лишь 4312 кДж/кг, т. е. в 5,5 раз меньше, чем необходимо для разрыва вышеуказанных связей [13]. Для гексогена для разрыва связей С–Н и С–N необходимо 19400 кДж/кг, а теплота взрывчатого разложения составляет 5740 кДж/кг, т. е. в 3,8 раза меньше. Для разрыва связей безводородного бензотрифуроксана (БТФ, бензо-трис (1,2,5-оксидиазолилоксид)) С–С и С=N необходимо 24600 кДж/кг, а теплота его взрыва составляет 5861 кДж/кг, т. е. в 4,2 раза меньше. Поэтому представления множества авторов, связанные с гомогенизацией “свободных” атомов углерода с последующей конденсацией их в аморфную углеродную фазу в сочетании с жидкока- пельной коалесценцией [8, 9] или с коагуляцией и кристаллизацией углерода на изоэнтропе расширения [14], или с конденсацией углерода из сильно пересыщенного пара по схеме пар–жидкость–кристалл [11, 12] вряд ли реальны в качестве единственного или основного механизма образования ДНА. Следует также отметить, что в случае кристаллизации образовавшихся капель жидко- го углерода начнется многоточечная кристаллизация алмаза с поверхности капель, а это не может привести к достаточно совершенной структуре кубического алмаза, который получается в результате детонационного синтеза.
Разрыв связей в молекуле ТНТ сопровождается отрывом метильной группы с образованием активного метильного радикала, нитрогруппы и фрагментацией бензольного кольца в “плазме” химпика (рис. 3).
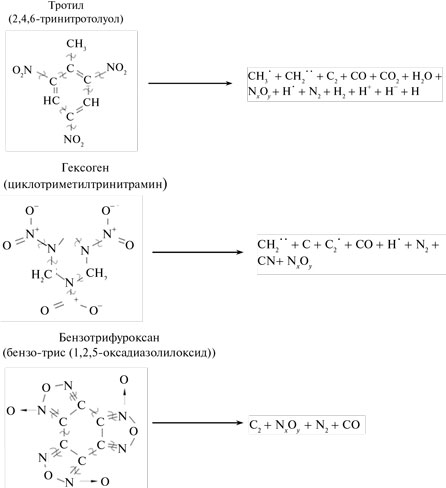
Рис. 3. Предполагаемый распад молекул ВВ в зоне химической реакции. ДНА образуется из ~ 95 % (по массе) углерода тротила и ~ 5 % (по массе) углерода гексогена.
Разрыв связей в молекуле гексогена пройдет по связям С–N. В молекулах БТФ идет разрыв по связям С–С и С=N. Наиболее важными компонентами “плазмы” для последующего образования алмаза из водородсодержащих углеродных ВВ являются радикалы, СН3, СН2, СН и относительно небольшое количество свободного углерода и соответствующих ионов. Из безводородного БТФ образуются следующие продукты: радикалоподобный димер С3, NxOy, N2 и СО. Из сопоставления видов радикалов, возникающих при детонационном разложении ТНТ, гексогена и БТФ, видно, что единственным радикалом, образующимся во всех трех процессах, является радикал С2 с неясным количеством свободных электронов и занятых водородом связей (для ТНТ и гексогена). Для БТФ занять свободные связи углерода водород не может, поскольку он отсутствует. Скорее всего, такой множественный ради- кал в момент образования, после распада молекулы БТФ, тут же вступает в реакцию с себе подобными или с растущей частицей ДНА.
Вероятно, существует не один, а несколько механизмов образования частиц ДНА. Образование первичных фрагментов будущих наноалмазов начинается от середины до конца зоны химической реакции (до плоскости Чепме — на — Жуге) из радикалов углеводородов. При этом образуется не бензольное ядро, а, возможно, циклогексан (энергетически наиболее выгодный). Небольшое количество капель жидкого углерода, образовавшихся из гексогена или БТФ по механизму жидкокапельной коалесценции, кристаллизуется или аморфизируется при расширении газообразных продуктов детонации (ПД) на первом этапе их расширения (на первом этапе изоэнтропы).
При изучении изотопного состава алмазосодержащей шихты, полученной при детонации октогена с ТНТ, меченым 13С по метильной группе было установлено, что основная часть ДНА в процессе детонационного синтеза образуется из углерода, входящего в состав ТНТ [15]. Аналогичный вывод был сделан при исследовании процесса синтеза из смеси гексогена и ТНТ меченым 14С в первое положение бензольного кольца ТНТ [16–20], при этом в образовании алмаза участвуют все атомы углерода ТНТ. При детонации сплава ТНТ/гексоген (50/50) наноалмазы образованы из углерода ТНТ и гексогена в соотношении 93/7 соответственно.
Как уже отмечалось, первичным “строительным блоком”, скорее всего, является радикалоподобный димер С2, вступающий в химическое взаимодействие с такой же частицей с образованием циклогексогена или сразу молекул адамантана (рис. 4).
Для водородсодержащих ВВ идет конкурентное образование кристаллита наноалмаза из радикалоподобного димера С2 и метильных радикалов, в част- ности из метильной группы ТНТ. Так, в зоне химической реакции образова- ние алмаза может идти через реакцию метильного радикала с радикалоподобной частицей адамантана аналогично CVD — методу получения алмазных пленок (о такой возможности указано в [21]). В газообразных ПД после за- вершения процесса синтеза ДНА из сплава ТНТ – гексоген обнаружено остаточное количество метана – 0,5–0,7 % (по массе) и водорода – 5,0–7,0 % (по массе) [18], что также может служить косвенным доказательством возможно- сти участия метильного радикала в процессе роста частицы ДНА (таблица) [22].
В [23] показано, что замена ТНТ в сплаве с гексогеном (60/40 соответственно) на тринитробензол (отсутствует метильная группа) при практически одинаковом массовом соотношении и близкой плотности заряда (1,65 и 1,69 г/см3 соответственно) приводит к падению выхода ДНА в 1,5 раза – с 8,4 до 5,48 % (по массе). При этом количество углерода в сплаве тринитробензол/гексоген уменьшилось незначительно – на 1,6 % (с 26,6 (ТНТ) до 25,0 (тринитробензол) % (по массе)). Таким образом, при использовании водородсодержащих углеродных ВВ метильный радикал ТНТ, скорее всего, играет очень важную роль в процессе образования наноалмаза.
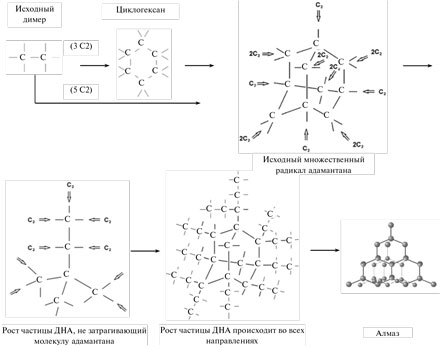
Рис. 4. Возможный механизм образования ДНА.
Экспериментальные данные по составу газовой среды во взрывной камере после пятого подрыва ТГ 40/60
| Газ | Состав газовой среды, % (по объему) | |||||
| воздух | азот | CO2 | ||||
| исходный состав | после подрыва | исходный состав | после подрыва | исходный состав | после подрыва | |
| CO2 | 0 | 11 | 0 | 7,6 | 41,6 | 21,0 |
| CO | 0 | 25 | 0 | 24 | 0 | 33,0 |
| O2 | 21 | 0,7 | 5,6 | 1,0 | 12 | 1,0 |
| H2 | 0 | 5,0 | 0 | 5,0 | 0 | 7,0 |
| N2 | 76 | 57 | 94,4 | 62 | 46,0 | 37,0 |
| CH4 | 0 | 0,52 | 0 | 0,5 | 0 | 0,5 |
Примечание. Масса каждого заряда ТГ 40/60 – 0,65 кг, ρ = 1,65 г/см3, объем камеры – 2,14 м3.
Рост частицы ДНА происходит по диффузионному механизму за счет химических реакций, протекающих на их поверхности при атаке свободными углеводородными радикалами. В процессе роста алмазной частицы ее поверхность постоянно покрыта углеводородными радикалами.
Что касается CVD-процесса, то по современным представлениям при использовании CH4 в среде водорода для получения алмазной пленки определяющую роль играет атомарный водород (в случае детонационного синтеза атомарный водород также образуется из водородсодержащих ВВ). При росте алмазной частицы атомарный водород, по сути, блокирует возможность свободных связей на углеродной поверхности растущей частицы алмаза образовывать двойные связи углерода друг с другом, образуя аморфизированную (графитовую) поверхность на частице. В процессе роста частицы водород заменяется на атакующий метильный радикал. Тем самым водород препятствует графитизации поверхности алмаза. Метильный радикал, присоединяясь к поверхности алмаза, переходит в sp3-гибридизированное состояние. Три атома водорода, входящие в состав метильного радикала, представляют собой три потенциальных места для присоединения следующих метильных радикалов.
Однако известно, что CVD-процесс получения наноалмазной пленки может быть осуществлен и без участия метильного радикала [24]. Так, была получена алмазная пленка из тетрахлорметана в присутствии катализаторов:
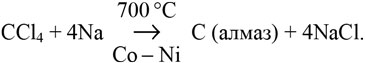
В [25] описана возможность получения алмазной пленки из метана, но в среде азота или аргона, что говорит об ином механизме образования алмазов в отличие от вышеописанного. Более того, некоторые авторы [3, 25] полагают, что основным радикалом CVD-процесса может быть димер С10.
В обычных условиях синтез адамантана достаточно сложен – это многостадийный синтез, в качестве исходных продуктов используют эфир Меервейна (тетраметиловый эфир бицикло[4,3,1]нонадион-2,6-тетракарбоновой- 1,3,5,7 кислоты) или димер циклопентадиена (метод Шлайера). Причем эти исходные продукты сами получаются достаточно сложно.
Адамантан – это насыщенный трициклический мостиковый углерод С10Н10. Молекула адамантана состоит из трех циклогексановых фрагментов, находящихся в конформации “кресло”. Пространственное расположение атомов углерода в молекуле адамантана повторяет расположение атомов в кристаллической решетке алмаза. Уникальность молекулы адамантана заключается в том, что она является жесткой и практически свободной от напряжений одновременно. Молекула адамантана обладает высокой симметрией и термостойкостью.
Обычно углеводороды, структура которых образована только σ-связями (как в случае адамантана), отличаются химической инертностью. Несмотря на это, адамантан и его производные весьма реакционноспособны. Например, адамантан-катион обладает высокой стабильностью по сравнению с другими третичными карбокатионами. Повышенная стойкость этого катиона связана с участием удаленных центров молекулы в делокализации заряда.
Важным обстоятельством является тот факт, что круг соединений, способных изомеризоваться в адамантановую структуру, очень широк. Алюминий (примесь к ВВ), который является катализатором таких изомеризаций, присутствует в небольших количествах в зоне химической реакции. Возникновение зародышей (возможно, адамантана) начинается в середине зоны химпика, а рост наноалмаза – также в середине ЗХР и заканчивается в начале разлета ПД.
Таким образом, ДНА образуются не столько при физических процессах, а в течение химических реакций, протекающих как в зоне химпика, так и сразу за плоскостью Чепмена-Жуге.
Рост частиц ДНА происходит по диффузному механизму за счет реакций присоединения димера С2 или метильного радикала, протекающих на его поверхности. Прекращение роста частиц ДНА происходит из-за действия двух факторов:
- накопления дефектов структуры по мере роста частицы и прекращения перехода sp2-гибридизированного углерода (С2 или метильного радикала) в sp3-гибридизированный “алмазный” углерод;
- исчерпывания углеродных радикалов вследствие их рекомбинации. Дело в том, что увеличение размера частиц ДНА вследствие их роста приводит к уменьшению удельной поверхности и, следовательно, к уменьшению количества вовлеченных в процесс радикалов. Начинают преобладать процессы рекомбинации радикалов.
ВЫВОДЫ
Процесс зарождения и роста частиц ДНА, скорее всего, носит исключи- тельно химический характер.
Авторы полагают, что образование ДНА имеет универсальный характер вне зависимости от используемого исходного углеродсодержащего ВВ – водородсодержащего (тротил, гексоген) или безводородного (бензотрифуроксан), при этом универсальной частицей для образования ДНА является ради- калоподобный димер С2.
Димер С2 является, скорее всего, причиной зарождения центра образования наноалмаза – радикалоподобной молекулы адамантана, предположительно, единственного стабильного образования углерода в зоне химической реакции.
Процесс роста кристаллита наноалмаза, по-видимому, происходит по диффузионному механизму за счет реакции присоединения димера С2 по свободным связям молекулы адамантана, а затем по свободным связям поверхности алмазной частицы.
Прекращение роста ДНА по предлагаемому механизму происходит из-за накопления дефектов структуры и прекращения перехода sp2-гибридизиро- ванного углерода в sp3-гибридизированный “алмазный” углерод, а также исчерпывания углеродных радикалов вследствие их рекомбинации.
Запропоновано новий механізм утворення частинок наноалмазу при детонаційному синтезі за наступною схемою: розпад молекул тринітротолуолу на основні радикали – радикалоподібний димер С2 і Н3, молекул гексогену – на С2, молекул бензотрифуроксану – на С2; утворення циклогексану з С2 або відразу молекули адаманта — ну в радикальній формі; взаємодія алмазоподібного ядра (радикала адамантану) з димером С2 і з метильними та іншими моноуглеродними радикалами; ріст частинок детонаційного алмазу аналогічно CVD-процесу. Показано, що зародження радикалоподібних молекул адамантану відбувається в діапазоні від середини зони хімпіка до площини Чепмена-Жуге, одночасно ростуть алмазні частинки, їх зростання завершується в початковій стадії ізоентропійного (тейлорівського) розширення газоподібних продуктів детонації, що захоплюють тверді частинки вуглецю.
In the present work we have suggested a new mechanism of formation of nanodiamond particles during detonation synthesis. The process diagram is following: decay of trinitrotoluene (TNT) molecules to basic radicals — radical-like dimer С2 and СН3, decay of hexo- gen molecules — to С2 ans benzotrifuroxane molecules – to С2; formation of cyclohexane from С2 or right away radical adamantane molecules; interaction of diamond-like core (adamantane radical) with methyl and other monocarbon radicals; growth of DND-particle like CVD-process. Origin of the radical-like adamantane molecule occurs over the range a center of chemical peak zone to the Chapman-Jouguet plane, growth of a diamond particle goes on in a starting stage of isentropic (Taylor) expansion of detonation gases, capturing solid carbon particles.
- Urizar M. J., James E., Smith L. C. Detonation velocity of pressed TNT // Phys. Pluids. – 1961. – 4, N 2. – P. 262–274.
- Van Thiel M., Ree F. H. Properties of carbon clusters in TNT detonation products: graphite– diamond transition // J. Appl. Phys. – 1987. – 62, N 5. – P. 1761–1767.
- Дремин А. Н. Першин С. В., Пятернев С. В., Цаплин Д. Н. Об изломе зависимости скорости детонации от начальной плотности ТНТ // Физика горения и взрыва. – 1989. – 25, No 5. – С. 141–144.
- Антипенко А. Г., Першин С. В., Цаплин Д. Н. Динамические исследования образования алмаза в продуктах детонации тротила // Proc. Xth Int. Conf. “High Energy Rate Fabrica- tion”, Ljubljana, Yugoslavia, 18–22 Sept., 1989. – Ljubljana, Yugoslavia, 1989. – P. 170– 178.
- Антипенко А. Г., Першин С. В., Цаплин Д. Н. Влияние фазового состояния углерода на электропроводность продуктов детонации тротила и его смесей с гексогеном // Химическая физика процессов горения и взрыва. Проблемы горения и взрыва, Черно- головка, 1989: Материалы IX Всесоюз. симп. по горению и взрыву. – Черноголовка, 1989. – С. 104–107.
- Першин С. В., Цаплин Д. Н., Антипенко А. Г. О возможности образования алмаза при детонации тетрила // V Всесоюз. совещание по детонации, Красноярск, 5–12 авг. 1991 г.: Сб. докл. – Черноголовка: Изд-во ИМТЕХ, 1991. – Т. 2. – С. 233–236.
- Першин С. В., Цаплин Д. Н. Динамические исследования детонационного синтеза плот- ных фаз вещества // V Всесоюз. совещание по детонации, Красноярск, 5–12 авг., 1991: Сб. докл. – Черноголовка: Изд-во ИМТЕХ, 1991. – Т. 2. – С. 237–243.
- Бабушкин Ю. А., Лямкин А. И., Чиганова Г. А., Ставер А. М. Численное исследование эволюции состава продуктов детонации в процессе детонационного синтеза алмаза // Ультрадисперсные порошки, наноструктуры, Красноярск, 17–19 дек. 1996 г.: Сб. докл. Межрегион. конф. с междунар. участием. – Красноярск: КГТУ, 1996. – С. 9–13.
- Бабушкин А. Ю., Лямкин А. И. О механизме образования ультрадисперсного алмаза при детонационном синтезе и зависимости его выхода от внешних условий // Физикохимия ультрадисперсных систем, Москва, 1999 г.: Сб. науч. тр. IV Всерос. конф., Москва, 1999 г.: МИФИ, 1999 г. – С. 125–128.
- Лямкин А. И. Образование наноалмазов при динамическом воздействии на углеродсодержащие соединения: Дис. … д-ра физ.-мат. наук. – Красноярск, 2007.
- Даниленко В. В. Фазовая диаграмма наноуглерода // Физика горения и взрыва. – 2005. – 41, No 4. – С. 110–116.
- Даниленко В. В. Особенности синтеза детонационных наноалмазов // Там же. – 2005. – 41, No 5. – С. 104–116.
- Долматов В. Ю. Детонационные наноалмазы. Получение, свойства, применение. – СПб: НПО “Профессионал”, 2011. – 536 с.
- Лобойко Б. Г., Любятинский С. Н. Зоны реакции детонирующих твердых взрывчатых веществ // Физика горения и взрыва. – 2000. – 36, No 6. – С. 45–64.
- Анисичкин В. Ф., Дерендяев Б. Г., Коптюг В. А. и др. Исследование процесса разложе- ния в детонационной волне изотопным методом // Там же. – 1988. – 24, No 3. – С. 121– 122.
- Козырев Н. В., Брыляков П. М., Сакович Г. В. и др. Исследование процесса синтеза ультрадисперсных алмазов методом меченых атомов // ДАН АН СССР. – 1990. – 314, No 4. – С. 889–891.




